ラットS100A9アッセイキット
カルプロテクチンは S100A8とS100A9の2つの蛋白質の複合体であり、炎症性腸疾患のバイオマーカーとして知られています。ヤマサ醤油では、ラットカルプロテクチン 構成蛋白質であるS100A9に対するモノクローナル抗体を用いてラットS100A9測定用ELISAを開発しました。本ELISAを用いてデキストラン 硫酸ナトリウム(DSS)誘発潰瘍性大腸炎(UC)モデルラットの糞便中S100A9を測定した結果、炎症早期からS100A9濃度が上昇し、UCモデル の良い指標となることが示唆されました1)。UCモデルラットにおけるS100A9について詳しくはこちらをご覧ください。
本ELISAをキット化して製品としたのが、ラットS100A9アッセイキットです。
●96穴マイクロプレートによるELISA法です。
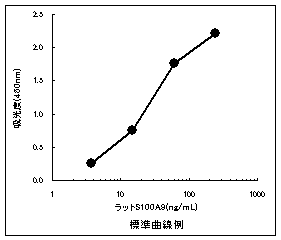
●ラットS100A9を3.75~240ng/mLの範囲で測定可能です。
●測定に必要な反応時間は一次反応2時間、二次反応1時間、発色反応20分です。
●ラット血清および糞便中※1のS100A9測定が可能です。※2
※1:糞便中S100A9の測定には、抽出操作が必要です。詳しくは「測定条の注意」の(1)をご参照下さい。
※2:試料は希釈して測定して下さい。詳しくは「測定上の注意」の(2)をご参照下さい。
2種類のマウス由来モノクローナル抗ラットS100A9抗体を用いたサンドイッチELSIAです。
●製品コード:80126
●本製品1キットに含まれる構成品:
| 構成品名 | 容量 | 数量 | |
|---|---|---|---|
| ① | 抗体固相プレート | 96穴マイクロプレート | 1枚 |
| ② | S100A9標準液1 (3.75ng/mL) | 0.5mL | 1バイアル |
| ③ | S100A9標準液2 (15ng/mL) | 0.5mL | 1バイアル |
| ④ | S100A9標準液3 (60ng/mL) | 0.5mL | 1バイアル |
| ⑤ | S100A9標準液4 (240ng/mL) | 0.5mL | 1バイアル |
| ⑥ | 希釈液(3倍濃縮液) | 25mL | 1バイアル |
| ⑦ | 洗浄原液(5倍濃縮液) | 50mL | 1バイアル |
| ⑧ | 酵素標識抗体 | 0.15mL | 1バイアル |
| ⑨ | 発色液A | 11mL | 1バイアル |
| ⑩ | 発色液B | 0.5mL | 1バイアル |
| ⑪ | 反応停止液 | 11mL | 1バイアル |
●貯蔵方法:2~8℃
●有効期間:製造日から18ヶ月
●希望小売価格:143,000円
<測定方法概要>
| 抗体固相プレートに標準液または検体を 100μLずつ分注 |
| ↓ 室温、2時間静置 |
| 反応液を除去後、調製済み洗浄液 300μLを各ウェルに分注 |
| ↓ 同操作を3回繰り返す |
| 反応液を除去後、調製済み標識抗体 100μLを各ウェルに分注 |
| ↓ 室温、1時間静置 |
| 反応液を除去後、洗浄液 300μLを各ウェルに分注 |
| ↓ 同操作を3回繰り返す |
| 調製済み発色液 100μLを各ウェルに分注 |
| ↓ 室温、20分静置 |
| 反応停止液 100μLを各ウェルに分注 |
| ↓ |
| 各ウェルの450nmでの吸光度を測定する |
(1)弊社にて検討に用いたラット糞便からの抽出方法例は下記の通りです。ご参考の上、目的にあった抽出方法をご検討下さい。
(1)抽出用希釈液の調製
キット添付の希釈液を精製水にて3倍に希釈した溶液に最終濃度0.5%(w/v)となるようにTriton X-100を加え、抽出用希釈液として使用します。
(2)使用器具
ペッスル、糞便回収用チューブ(ペッスルを差し込める口径の物)など
(3)抽出方法
1) 予め各糞便回収用チューブの重量を測定しておきます。
2) 200mg前後の便を糞便回収用チューブに回収します。
3) 回収後重量を測定し、チューブの重量を差し引き、便の重量を算出します。
4) 糞便回収用チューブに抽出用希釈液を500μL加えて、15分静置します。
5) ペッスルを使用し、便を粉砕して良く攪拌します。
6) 抽出用希釈液500μLでペッスルを洗いながら、全ての残物を回収します。
7) 4℃、12,000×gで 5分間遠心し、上清を別チューブに回収します。
8) 上清を抽出用希釈液にて10倍以上に希釈します。
9) 標準操作法により上清中のS100A9濃度を求め、糞便1mg当たりのS100A9を算出して下さい。
(2)試料は添付の希釈液にて希釈してから測定して下さい。ラット血清および糞便抽出液共に10倍希釈が目安です。測定範囲以上の濃度を示す試料ついては、適宜希釈して下さい。
(3)その他ご不明な点は、診断薬営業情報室までお問い合わせ下さい。
1. 村山 寛 他 : 第42回日本毒性学会
2. Sekiya S et al. (2016). J Immunol Methods. 439. 44–49.